人工核酸スクリーニングプロジェクト
1.メンバー
| プロジェクトリーダー | 笠原 勇矢 |
|---|---|
| プロジェクト研究員 | 星野 秀和 |
| 特任研究員 | 石田 健太 |
| 技術補助員 | 山隈 晴美、千賀 陽子、亀岡 なつ実、阿曽 古都美 |
| 客員研究員 | 朴 昭映、織田 昌幸、稲垣 匡子 |
| 連携大学院生 | 三田村 澪 (D1) |
| 研修生 | 尾田 ちひろ (D2)、爲則 裕介 (B6)、仁田峠 海斗 (D1)、吉村 駿佑 (B5)、飯沼 宏太 (B3) |
2.研究目的・背景
近年、化学技術の発展により、人工的に作製した核酸(Xeno nucleic acid; XNA)を医薬品として利用することが可能になってきており、これまでに16種類の核酸医薬が日米欧で承認されています。例えば、「Spinraza」や「Viltepso」などのアンチセンス核酸や、「Onpattro」などのsiRNAは、標的mRNAに配列特異的に作用し疾患原因となるタンパク質への翻訳を制御することで薬効を示す核酸医薬です。また、「Macugen」は、アプタマーと呼ばれ、疾患原因となるタンパク質に構造特異的に作用し活性を制御する核酸医薬です。このように核酸医薬には様々なタイプのものがあり、DNAやRNA、タンパク質など生体内に存在するほとんどの分子を標的にすることが可能なため、既存の手法では治療が困難な難治性疾患に対する特効薬開発につながると期待されています。
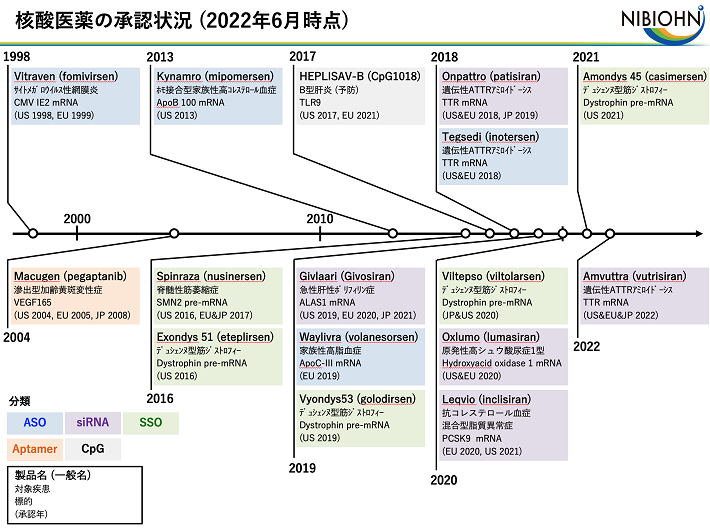
人工核酸スクリーニングプロジェクトでは、アンチセンス核酸やアプタマーなどの核酸医薬品に導入する人工核酸の合成や配列のデザイン、スクリーニングによる標的特異的な核酸分子の単離と機能評価、用途に応じた最適化を行うことで、核酸医薬品の創出に取り組んでいます。
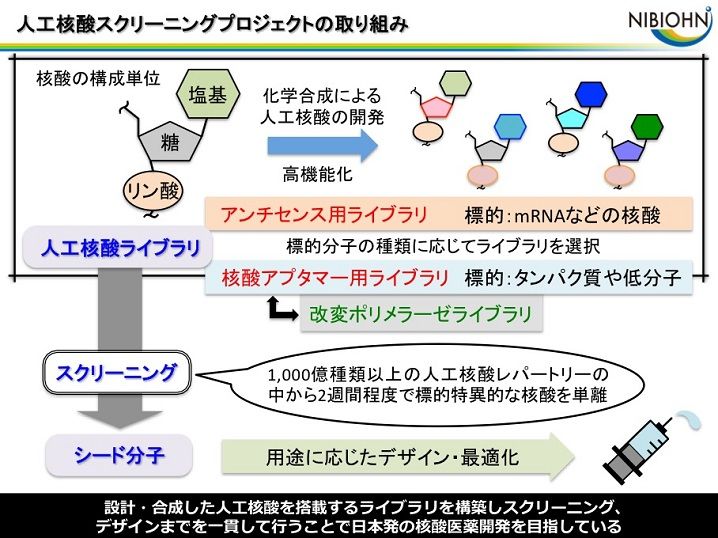
3.研究内容
優れたアンチセンス核酸には、標的RNAに対する結合親和性や生体内安定性、細胞内移行性、安全性などの特性が求められます。同様に、優れた核酸アプタマーの創出には、生体内安定性や安全性だけでなく標的タンパク質に対する結合親和性や阻害活性、体内滞留性などを考慮することが必要です。これらの特性を付与するために、核酸の塩基部、糖部、リン酸部を修飾した人工核酸を開発しています。また、候補配列ライブラリの中から活性配列を高効率に選別可能な新規スクリーニング手法の開発も進めています。特に核酸アプタマーのスクリーニングにおいては、ポリメラーゼに人工核酸を認識させることが必須であるため、それを可能とする改変ポリメラーゼの開発を進めています。このように、人工核酸の合成からスクリーニングまでを一貫して行うことで人工核酸の可能性を引き出し、難治性希少疾患を始めとする様々な疾病に対する核酸医薬開発を目指した研究を行っています。
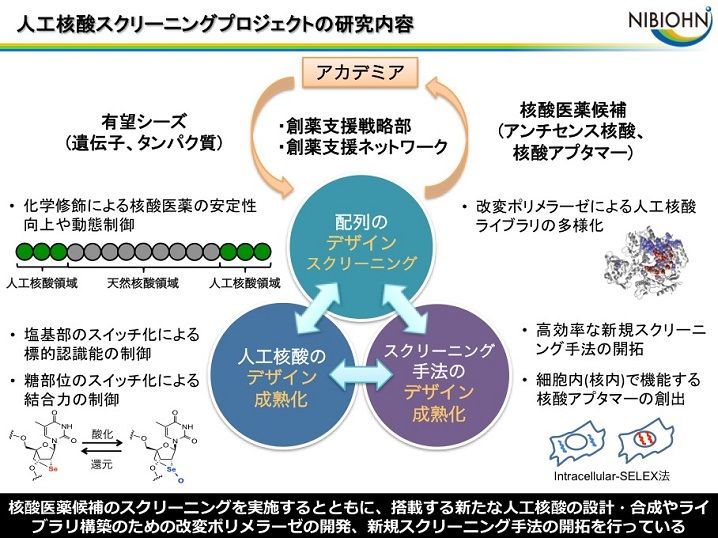
研究課題
1) 人工核酸を高効率に導入可能な改変ポリメラーゼの開発
2) 核酸医薬品創出へ向けた新規スクリーニング手法の開拓
3) Aptamer Based Drug Design(ABDD)創薬プラットフォームの構築
4) 細胞内移行性人工核酸アプタマーの創出
最近の主要論文
- Yoshida T, Morihiro K, Naito Y, Mikami A, Kasahara Y, Inoue T, Obika S. Identification of nucleobase chemical modifications that reduce the hepatotoxicity of gapmer antisense oligonucleotides. Nucleic Acids Res, 2022, 50(13):7224-7234.
- Ii H, Kasahara Y, Yamaguma H, Kageyama S, Kawauchi A, Obika S, Susumu N, Systemic Administration of Gapmer-type Antisense Oligonucleotides Targeting γ-Glutamylcyclotransferase Suppresses The Growth of A549 Human Lung Cancer Xenografts, Anticancer Res, 2022, 42(3):1221-1227.
- Uemachi H, Kasahara Y, Tanaka K, Okuda T, Yoneda Y, Obika S. Hybrid-type SELEX for the selection of artificial nucleic acid aptamers exhibiting cell internalization activity, Pharmaceutics, 2021, 15;13(6):888.
- Hoshino H, Kasahara Y, Kuwahara M, Obika S. DNA polymerase variants with high processivity and accuracy for encoding and decoding locked nucleic acid sequences. J Am Chem Soc, 2020, 23;142(51):21530-21537.
- Tanaka K, Okuda T, Kasahara Y, Obika S. Base-modified aptamers obtained by cell-internalization SELEX facilitate cellular uptake of an antisense oligonucleotide. Mol Ther Nucleic Acids, 2020, 23:440-449.
- Uemachi H, Kasahara Y, Tanaka K, Okuda T, Yoneda Y, Obika S. Discovery of cell-internalizing artificial nucleic acid aptamers for lung fibroblasts and targeted drug deliver. Bioorg Chem, 2020, 105:104321.
- Kanda M, Kasahara Y, Shimizu D, Miwa T, Umeda S, Sawaki K, Nakamura S, Kodera Y, Obika S. Amido-bridged Nucleic Acid-modified Antisense Oligonucleotides Targeting SYT13 to Treat Peritoneal Metastasis of Gastric Cancer. Mol Ther Nucleic Acids, 2020, 22:791-802.
- Okuda T, Kawashima Y, Kasahara Y, Takagi T, Yamamoto J, Iwai S, Obika S. Inhibiting guanine oxidation and enhancing the excess-electron-transfer efficiency of a pyrene-modified oligonucleotide by introducing an electron-donating group on pyrene. Chem Commun (Camb), 2019, 55(93):14062-14065.
- Matsumoto S, Yamamichi T, Shinzawa K, Kasahara Y, Nojima S, Kodama T, Obika S, Takehara T, Morii E, Okuyama H, Kikuchi A. GREB1 induced by Wnt signaling promotes development of hepatoblastoma by suppressing TGFβ signaling. Nat Commun, 2019, 10(1):3882.
- Uehara T, Choong CJ, Nakamori M, Hayakawa H, Nishiyama K, Kasahara Y, Baba K, Nagata T, Yokota T, Tsuda H, Obika S, Mochizuki H. Amido-bridged nucleic acid (AmNA)-modified antisense oligonucleotides targeting α-synuclein as a novel therapy for Parkinson's disease. Sci Rep, 2019, 9(1):7567.
人工核酸スクリーニングプロジェクト
| y-kasahara※nibiohn.go.jp (※を@に置き換えてください。) |
