III�������@�A�K�i�y�ю������@�A���萫����
�{���ȍ~�́A�O�y�[�W�̊J���v���Z�X�����������̂ł��B�V���i�̐����̔��̏��F���悤�Ƃ���Ƃ��́A���́u�L�����v�A�u���S���v�y�сu�i���v�𗠂Â��邽�߂̎������ю���(�Q�ƃy�[�W��)�������J���Ȃɒ�o���邱�ƂɂȂ�܂��B�����̎����̎��W���@�Ȃǂɂ��ẮA���ۓI���a��}��ړI��1990�N�ɑg�D���ꂽ����EU���i�K�����a���ۉ�c(ICH)�ɂ����āA����܂łɐ������̃K�C�h���C���Ƃ��Ď�����Ă��܂��B�{���ɂ����ẮA�u�i���v�Ɋ֘A����d�v�����ɂ��ĉ�����܂��B�Ȃ��A���w�����i�̕i���Ɋւ�����ICH�K�C�h���C���ɂ��ẮA�{�͕\1���Q�Ƃ��ĉ������B
1.���i�̕i���ۏ�
���i�̕i���ۏ́A�Տ������ɂ����Ċm�F���ꂽ�L�����ƈ��S����Տ�����ɂ����Ă��ۏ��邽�߂̎肾�ĂƂȂ���̂ł��B���i�̏��F�\�����ɂ́A����y�ѐ��܂ɂ��Ă��ꂼ�ꐻ�����@�A�K�i�y�ю������@�A���тɈ��萫�����Ɋւ��鎑���̒�o���K�v�ƂȂ�܂��B�Ȃ��A�{�����Ō���Ƃ́A���܂̐��Y�Ɏg�p���邱�Ƃ�ړI�Ƃ��镨���ŁA���܂̐����Ɏg�p���ꂽ�Ƃ��ɗL�������ƂȂ���̂ł��B
2.����
(1)�������@
���F�\�����ɂ́A���F�\�����ɐ����ꏊ�y�ѐ������@���L�ڂ���K�v������܂��B�������@�ɂ��ẮA�o�����������H���܂ł̈�A�̍H������̓I�ɋL�ڂ��邱�Ƃ��K�v�ł���A�����H���̒��ł��i���m�ۂɓ��ɏd�v�ȍH���y�ђ��ԑ̂����ꂼ��d�v�H���y�яd�v���ԑ̂Ƃ��āA���̍H������̊T���A�v���Z�X�p�����[�^�A�H���Ǘ����������܂߂ċL�ڂ��邱�ƂƂȂ��Ă��܂��i�u�����@�Ɋ�Â����i���̐����̔����F�\�����L�ڎ����Ɋւ���w�j�ɂ��āv�iH17.2.10 ��H�R����0210001�j�Q�Ɓj�B���F�\�����ɋL�ڂ����������@�́A���F�\�����ɓY�t���鐻�����@�̊J���̌o�܁A�������@�̃o���f�[�V�����f�[�^���Ɋւ��鎑���ɂ��A���̉Ȋw�I�Ó������������K�v������܂��B�R���ɂ����ẮA��o���ꂽ�����̉Ȋw�I�Ó������m�F����A�܂��AGMP�����ɂ����Ď��ۂ̐����ꏊ�ł̐����H���A�����Y�ł̃o���f�[�V�����f�[�^�����m�F����܂��B
(2)���܂̐����ƃ��X�N�Ǘ�
���ȕi���̐��܂���т��ċ������邽�߂ɂ́A�������ꂽ���܂��������邱�Ƃɂ���Ă��̕i����ۏ���̂ł͂Ȃ��A����������i������荞�ނ悤�ɐ����H�����J�����H���Ǘ����s�����ƁA�܂��J�����ɐ����H���ɂ��Ă̑̌n�I�Ȓm����ςݏグ�čH���̋��e�\�͈͂Ɋւ�����Ă������Ƃɂ��A�����Y�Ɉڍs���Ă���̐��@�ύX�ɏ_��ɑΉ��ł���悤�ɂȂ邱�Ɠ��̍l�������u���܊J���Ɋւ���K�C�h���C���v�iQ8�j�Ɏ�����Ă��܂��B�܂��A�u�i�����X�N�}�l�W�����g�Ɋւ���K�C�h���C���v�iQ9�j�ł́A�����I���P��I�ɓK���ȕi���̈��i�����苟�����邽�߂ɗ��p�\�ȃ��X�N�Ǘ��̑̌n�I�A�v���[�`����Ă���Ă��܂��BQ8�y��Q9�́A�i���ۏ̍l�����̐V���ȍ��ۓI�����ƂȂ��Ă��܂��B
3.�K�i�y�ю������@
�K�i�y�ю������@�Ƃ́A����y�ѐ��܂̕i�����m�ۂ��邽�߂̎������@�y�ю����������Ƃ��̓K�ۂ̔��������������̂ł��B���w�����ɂ��V���i�̋K�i�y�ю����@�̐ݒ�Ɋւ���W���I�ȍl�����ɂ��ẮA�u�V���i�̋K�i�y�ю������@�̐ݒ�ɂ��āv(Q6A)�Ɏ�����Ă��܂��B�K�i�y�ю������@�̐ݒ�ɍۂ��ẮA���{��Ǖ��̒ʑ��A���ܑ����A��ʎ����@�A�W���i�y�ю���E���t�������p���邱�Ƃ������Ƃ��܂��B�K�i�������ڂƂ��ẮA���́A�\�������͎������A���q���y�ѕ��q�ʁA��A�ܗʋK�i�A����A�m�F�����A�����l�i�����I���w�I�������j�A���x�����A�����ܗʁi�������͊������ʁj�A���M�c���A�D�����͎_�s�n���D���A�������A���ꎎ���A���̑��̎������ځi���������x�����A����̗��q�a���܂ށj�A��ʖ@��������܂��B��ɂ��ẮA���w�\�����蕨�͋L�ڕs�v�ł����A�d���́A����A���퐻�܂�y�f���܂ł͕K���L�ڂ��܂��B�ܗʋK�i�́A�����ߒ��A��ʌ덷�y�ш��萫���Ɋ�Â��A�L�����ƈ��S���Ɋւ��ē����Ƃ݂Ȃ���K�i�l��ݒ肷����̂ŁA����l�Ɖ����l���߂܂��B����Ƃ́A����ł���Ό`��(�ő́A�t��)�A�F�Ȃǂł��B�m�F�����́A���Y���i���ړI���ł��邩�ۂ����m�F���鎎���ł��B�����l�́A�z���x�A�����x�ApH�y�їZ�_�Ȃǂł��B���x�����́A�L�@����@�s�����y�юc���n�}�̊�l�Ɋւ���K�C�h���C���iQ3A�AQ3B�AQ3C�j���Q�l�ɁA�X�̈��i�Őݒ肷�ׂ����ڂf���܂��B�K�i���ڂɂ́A����A�m�F�����A��ʖ@�y�я��x�����̂悤�ɊT�ˑS�Ă̌��͐��܂ɓK�p�������̂ƁA�����l��n�o���y�ѐ��܋ψꐫ�̂悤�ɁA�e���͐��܂̓����ɉ����Đݒ肷����̂�����܂��B�R���ɂ����ẮA���̈��i�̓����܂�����ŁA�i����ۏ��邽�߂ɓK�ȋK�i�������ځA�������@�y�ыK�i�l���ݒ肳��Ă��邩�ǂ������A�ݒ荪���Ƃ��Ē�o���ꂽ��������Ɋm�F���܂��B
4.���萫����
�V�L�������ܗL���i�̈��萫�����́A�u���萫�����K�C�h���C���v(Q1A(R2))�Ɋ�Â����{����܂��B���x�A���x�A�����̗l�X�Ȋ����q�̉e���̉��ł̕i���̌o���I�ω���]�����A����ɂ��Ă͒��������A�y�їL�����Ԗ��̓��e�X�g����(���Y�����܂̐����Ɏg�p�ł�����ԁB���e�X�g���Ԃ�������́A���ܐ������ɍĎ��������{���K�i�ւ̓K�������m�F���邱�Ƃ��K�v)�A���܂ɂ��Ă͒��������y�їL�����Ԃ̐ݒ�ɕK�v�ȏ��邽�߂̎����ł��B
(1)����̈��萫����
�@�Ս�����
�悸�Ս������ɂ��A����̈��萫�v���t�@�C���ɂ��Ă����悻�̏������݂܂��B�������̓���╪���o�H�f����̂ɖ𗧂Ƌ��ɁA���萫�����ɗp���镪�͖@�̓K�������m�F���邱�Ƃ��ł��܂��B�ʏ�A�����A�����x�A�_���A���ɂ��e�����������܂��B�����萫�����̏����́u�V����y�ѐV���܂̌����萫�����K�C�h���C���ɂ��āv�iQ1B�j�ɒ�߂��Ă��܂��B
�A�����ۑ������y�щ�������
����ɂ��Ă̓p�C���b�g�X�P�[���ȏ�Ő������ꂽ3���b�g�ȏ�ɂ��Ď��������{���܂��B���荀�ځA���͕��@�y�є����̓K�C�h���C��Q6A�y��Q6B�i�\3�Q�Ɓj�ɋL�ڂ���A���̕������̋K�i��Q3A(R2)�Ř_�c����Ă��܂��B�ۑ������́A��ʓI�Ȍ���̒����ۑ������ł͉��x�A���x��25���}2���A60��RH�}5%RH����30���}2���A60��RH�}5%RH�Ƃ���12�����i�\�����_�ł̍ŒZ�������ԁj�ȏ�A���������ł͉��x�A���x��40���}2���A75��RH�}5%RH�Ƃ���6�����ł��B
(2)���܂̈��萫����
�����ۑ������y�щ��������́A3���b�g�ȏ�̎s�̗\�萻�܂Ɠ��ꏈ���A����e��{���n�̕�ōs���܂��B���荀�ځA���͕��@�y�є����́A�K�C�h���C��Q6A�y��Q6B�ɋL�ڂ���A���ܒ��̕������̋K�i��Q3B(R2)�Ř_�c����Ă��܂��B�ۑ������́A��ʓI�Ȑ��܂̒����ۑ������ł͉��x�A���x��25���}2���A60��RH�}5%RH����30���}2���A60��RH�}5%RH�Ƃ���12�����i�\�����_�ł̍ŒZ�������ԁj�ȏ�A���������ł͉��x�A���x��40���}2���A75��RH�}5%RH�Ƃ���6�����ł��B�܂��A�����萫�����͕K�v�ɉ����Đ��܂�1�ȏ�̃��b�g�ɂ��čs���܂��B
(3)���萫�����p�����̐\��
12�����ȏ�̒����ۑ������f�[�^������Έ��萫�����̓r���ł��\���͉\�ł��B���̏ꍇ�A���̎��_�܂łɓ����Ă�����萫�����f�[�^�Ɋ�Â����b��I�ȗL�����Ԃ�ݒ肷��K�v������܂��B
5.�V�Y������z������ꍇ�̎戵��
�����F���i���̓Y�����Ƃ��Ă̎g�p�O�Ⴊ�Ȃ��Y������z������ꍇ���͎g�p�O�Ⴊ�����Ă����^�o�H���قȂ�Ⴕ���͑O�������ʂ��g�p����ꍇ�ɂ́A���Y�Y�����̕i���A���S�����Ɋւ��鎑�����Ē�o���Ȃ���Ȃ�܂���B�R���ɂ����ẮA���Y�Y�����̕i���y�ш��S���ɂ��Ċm�F���A�\�����܂̓��������܂�����ŁA���̓Y�������g�p���邱�Ƃ̉ۂf���܂��B
�\1�@���w�����i�̕i���Ɋւ�����ICH�K�C�h���C��
| ���� | �g�s�b�N | �K�C�h���C���� | �����ʒm |
|---|---|---|---|
| ���萫 | Q1A(R2) Q1B |
���萫�����K�C�h���C�� �V����y�ѐV���܂̌����萫�����K�C�h���C�� |
H15.6.3 ���R��0603001 H9.5.28 ��R422 |
| �s���� | Q3A(R2) Q3B(R2) Q3C(R3) |
�V�L�������ܗL���i�̂�������̕s�����Ɋւ���K�C�h���C�� �V�L�������ܗL���i�̂������܂̕s�����Ɋւ���K�C�h���C�� ���i�̎c���n�}�K�C�h���C�� |
H14.12.16 ���R����1216001�A H18.12.4 ��H�R����1204001 H15.6.24 ���R��0624001�A H18.7.3 ��H�R����0703004 H10.3.30 ���R307 |
| �K�i�y�ю������@ | Q6A | �V���i�̋K�i�y�ю������@�̐ݒ� | H13.5.1 ���R��568 |
| ���܊J�� | Q8 | ���܊J���Ɋւ���K�C�h���C�� | H18.9.1 ��H�R����0901001 |
| �i�����X�N�}�l�W�����g | Q9 | �i�����X�N�}�l�W�����g�Ɋւ���K�C�h���C�� | H18.9.1 ��H�R����0901004�A H18.9.1��H�Ė���0901005 |
���p���Ɍ����Č����҂��m���Ă����ׂ����ƂƂ́H
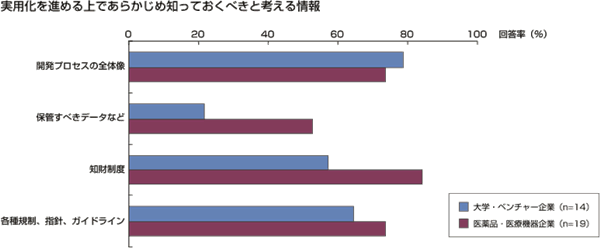
�����̐����Ɠ���ΏۂɎ��{���ꂽ�����ɂ��ƁA���p���Ɍ������������s���ɓ������ăx���`���[��Ƃ��w�̌����҂��Œ���F�����Ă����ė~�����Ɗ�]������̏�ʂ��߂����ڂ́A�u�m�I���Y���x�v�A�u�e��̋K���E�K�C�h���C���v�A�u���i�J���v���Z�X�̑S�̑��v�A�u�ۊǂ��Ă����ׂ��f�[�^���v�ł������B���̌X���́A��w�����ҁE�Y�w�A�g�R�[�f�B�l�[�^�[�A�x���`���[��Ƃɑ��čs��ꂽ���l�̒����ɂ����Ă������̍��ڂŔF�߂�ꂽ���̂́A���Ɂu�m�I���Y���x�v�Ɓu�ۊǂ��ׂ��f�[�^���v�Ɋւ�����̏d�v���ɂ��Ă͐����Ƒ��̈ӎ�����荂���X���ɂ���B
�u�ۊǂ��ׂ��f�[�^���v�ɂ��Ă͏��F�\���̍ۂɁA�u�m�I���Y���x�v�ɂ��Ă͎s��ł̓Ɛ萫���m�ۂ���ۂɂ��ꂼ��d�v�ȃt�@�N�^�[�ƂȂ邱�Ƃ���A��w���̌����҂����p�������������������s���ۂɂ͓�������C��z���Ă������Ƃ��d�v�ł���Ƃ�����B
(����18�N�x�����J���Ȋw������⏕�����i�E��Ë@��J���ɑ��闝�i�Ɋւ��錤��(��C�����ҁF���R���L)���)