バイオ創薬プロジェクト
1.メンバー
| プロジェクトリーダー | 鎌田 春彦(併任) |
|---|---|
| プロジェクト研究員 | 中山 泰亮(併任) |
| 特任研究員 | 新山 真由美(併任) |
| 技術補助員 | 竹島 まどか、岡部 章子、山中 結子、佐藤 玲子 |
| 客員研究員 | 井上 豪、内山 進 |
| 協力研究員 | 井上 雅己 |
| 事務補助員 | 香取 美穂 |
2.研究目的・背景
近年、抗体やサイトカイン、生理活性ペプチド、核酸といったバイオテクノロジー産物が、画期的な次世代医薬(バイオ医薬)として開発、実用化されつつあり、がんや自己免疫疾患など、従来型の医薬品では治療が困難であった難治性疾患(難病)も、不治の病から治せる病へとパラダイムシフトしてきています。しかし、このようなバイオ医薬の開発プラットフォームは、未だ発展途上であり、治療法の確立されていない難病に対して、より有効性と安全性、そして品質が高度に保証された、効果に優れた医薬品として開発するための基盤技術の開発が強く求められています。本プロジェクトでは、我々独自のプロテオーム解析技術やタンパク質工学技術を駆使することにより、難治性疾患に対する新しい治療法の開発を目指しています。
3.研究内容
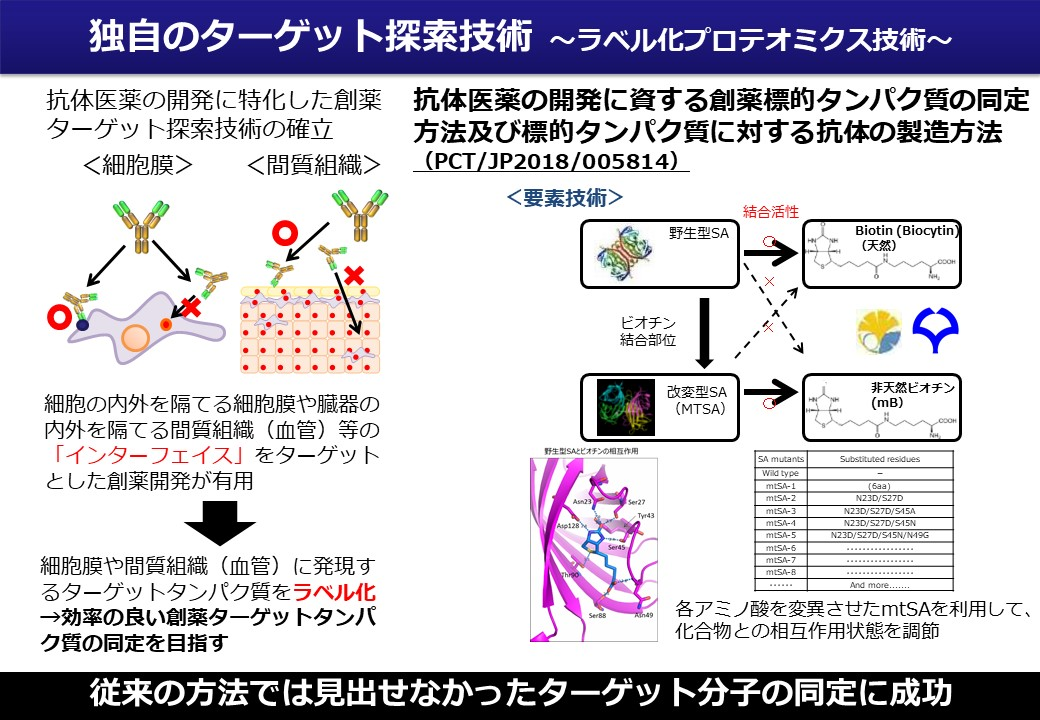
(1) ラベル化試薬を活用した抗体医薬の開発に資する創薬標的探索技術の確立
病態組織の細胞膜上に発現する膜タンパク質は、抗体医薬の創薬ターゲットとして重要な分子である。そのため、膜タンパク質の解析が、様々な手法を用いて行われているが、抗体医薬のターゲットとして、実際に探索に成功した例は殆どない。その理由として、 ①創薬標的として抗体が到達する部分に多く発現する分子が特定されていない、②病態細胞の膜タンパク質の解析に終始し、細胞・組織の局所的な発現動態に着目していない、等の原因が考えられる。そこで、我々はこれらの問題を解決すべく、新規ラベル化試薬を用いた創薬ターゲットの同定を試みている。我々は、組織中に含まれる多量タンパク質の排除を目的として、新規ラベル化化合物とそのラベル化化合物特異的に結合する変異タンパク質の作製を通じて、創薬ターゲットの探索に取り組んでいる。特に、これらの化合物を、モデル動物等に対して還流させる「in vivoラベル化技術」を適応し、実際に抗体医薬を投与した際の、動態特性にも念頭においた創薬ターゲット探索に取り組んでいる。
(2) 新規フォーマットを持つ抗体誘導体の開発
抗体医薬の開発においては、新規のフォーマットを持つ抗体誘導体の作製が、実用化に向けて有利なアプローチとなる。我々は、体内に存在するタンパク質の中から、必要な薬物を効率よく送達するための基盤技術を開発している。近年、抗体-薬物複合体(Antibody-Drug Conjugate:ADC)をはじめとする、様々な抗体誘導体が作製され、臨床応用されつつある。これらの抗体誘導体の開発技術については、既に開発済みのものを含めて、科学的な合理性の乏しい研究分野でもある。我々は、今後の次世代抗体医薬の台頭を見越して、新しいフォーマットを持つ抗体医薬の開発を進めている。特に、我々は、がんのアクティブターゲティング技術として開発が進むADCを念頭に、新しい抗体フォーマットの作製を進めている。

4.参考文献
- Higashisaka K, Takeya S, Kamada H, Obana M, Maeda M, Kabayama M, Yamamoto K, Ishida N, Isaka R, Tsujino H, Nagano K, Tomiyama N, Rakugi H, Fujio Y, Kamide K, Tsutsumi Y., Identification of biomarkers of chronic kidney disease among kidney-derived proteins, Clin Proteomics 19, 3 (2022)
- Yamaguchi T, Hoshizaki M, Minato T, Nirasawa S, Asaka MN, Niiyama M, Imai M, Uda A, Chan JF, Takahashi S, An J, Saku A, Nukiwa R, Utsumi D, Kiso M, Yasuhara A, Poon VK, Chan CC, Fujino Y, Motoyama S, Nagata S, Penninger JM, Kamada H, Yuen KY, Kamitani W, Maeda K, Kawaoka Y, Yasutomi Y, Imai Y, Kuba K., ACE2-like carboxypeptidase B38-CAP protects from SARS-CoV-2-induced lung injury. Nat Commun. 12:6791. (2021)
- Urano E, Okamura T, Ono C, Ueno S, Nagata S, Kamada H, Higuchi M, Furukawa M, Kamitani W, Matsuura Y, Kawaoka Y, Yasutomi Y. COVID-19 cynomolgus macaque model reflecting human COVID-19 pathological conditions. Proc Natl Acad Sci U S A. 118:e2104847118. (2021)
- Asaka MN, Utsumi D, Kamada H, Nagata S, Nakachi Y, Yamaguchi T, Kawaoka Y, Kuba K, Yasutomi Y., Highly susceptible SARS-CoV-2 model in CAG promoter-driven hACE2-transgenic mice. JCI Insight.;6:e152529. (2021)
- Akiba H, Ise T, Nagata S, Kamada H, Ohno H, Tsumoto K., Production of IgG1-based bispecific antibody without extra cysteine residue via intein-mediated protein trans-splicing, Sci. Rep. 11, 19411 (2021).
- Inoue M, Yamashita K, Tsuji Y, Miki M, Amano S, Okumura T, Kuge K, Tone T, Enomoto S, Yoshimine C, Morita Y, Ando D, Kamada H, Mikami N, Tsutsumi Y, Tsunoda SI. Characterization of a TNFR2-Selective Agonistic TNF-α Mutant and Its Derivatives as an Optimal Regulatory T Cell Expander. J Immunol. 206, 1740-1751. (2021)
- Inoue M, Tsuji Y, Yoshimine C, Enomoto S, Morita Y, Osaki N, Kunishige M, Miki M, Amano S, Yamashita K, Kamada H, Tsutsumi Y, Tsunoda SI., Structural optimization of a TNFR1-selective antagonistic TNF-α mutant to create new-modality TNF-regulating biologics. J Biol Chem. :jbc.RA120.012723. (2020)
- Kamada H., Search for drug discovery targets focusing on cancer stroma., Translational and Regulatory Sciences, 1 58-65, (2019)
バイオ創薬プロジェクト
| ウェブサイト | https://www.nibiohn.go.jp/bio-r/ |
|---|---|
| kamada※nibiohn.go.jp (※を@に置き換えてください。) |
