国立研究開発法人 医薬基盤・健康・栄養研究所
国立研究開発法人 医薬基盤・健康・栄養研究所
免疫老化プロジェクト
免疫老化プロジェクト

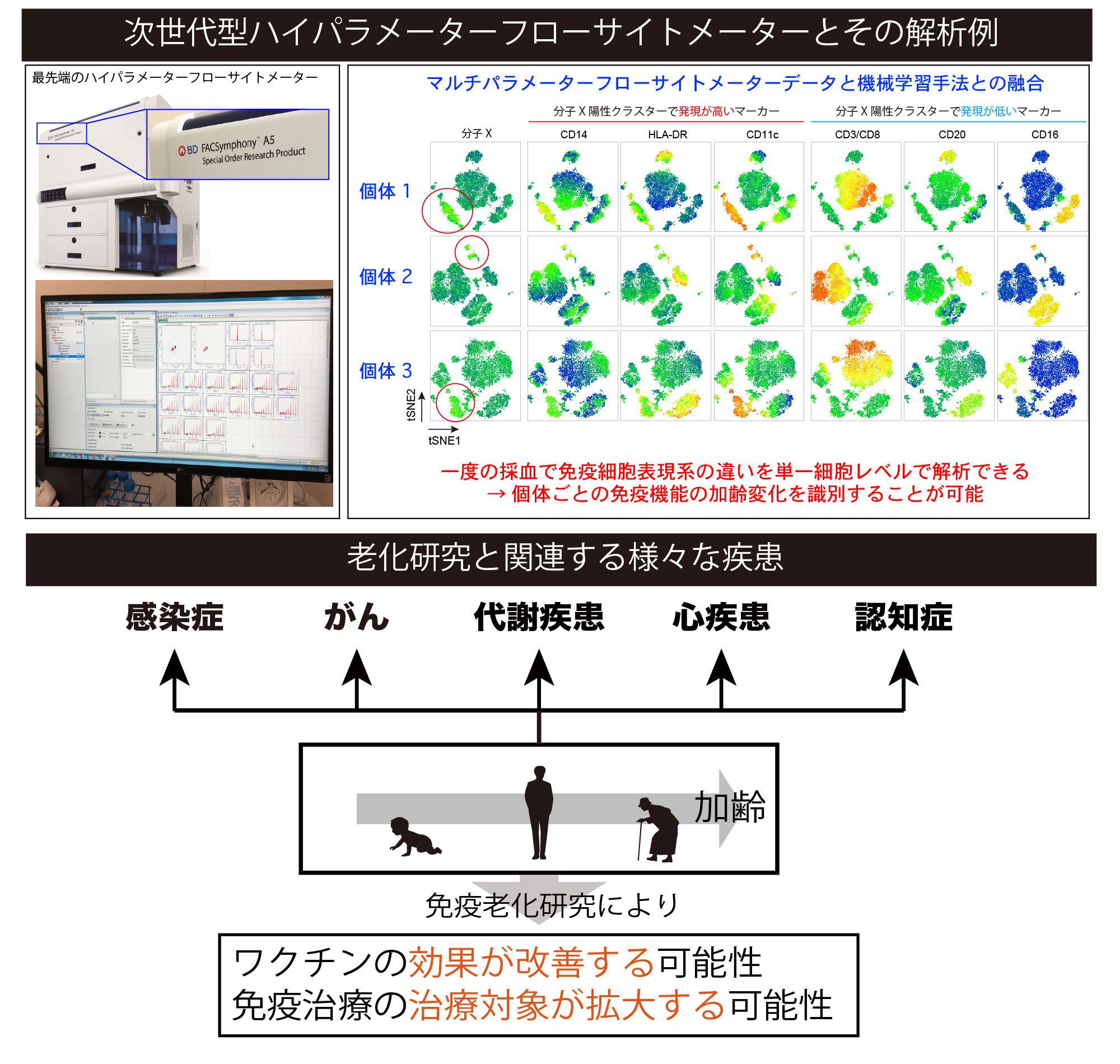
生命システムにおいて、細胞レベルでの細胞老化現象に加え、加齢に伴う免疫システムの個体レベルでの変化、いわゆる免疫老化という現象が近年注目されています。この免疫老化に関連する事象として、一般的にヒトでは65歳以上の高齢者で、がん、感染症等による死亡率が急激に上昇することが知られています。つまり加齢に伴うヒトの生涯を通した免疫反応の経時的変化を理解、検討する事により、今後の新しい概念に基づくワクチン開発や免疫療法の確立へと繋がることが期待されます。しかしながら純粋な加齢に伴う免疫老化の本態に関しては未解明な点が多いのが現状です。 我々はこれまで、フランスINSERM Dr. Appayのグループとの共同研究により、ヒト末梢血単核細胞(PBMC)を用いたex vivo解析で、加齢に伴ってNaïve T細胞が減少すること、高齢者由来造血幹細胞のテロメラーゼ活性の低下や分化異常が見られ、その後に分化誘導されたリンパ球系細胞のテロメラーゼ活性が低下していることを世界に先駆けて見出しています。 現在ではヒトの免疫系と極めて近縁であると考えらえる霊長類カニクイザルモデルを用いて、個体レベルでの解析により、免疫老化という事象の全体像を把握することを目指し研究しています。また、我々は日本BD社と連携し、次世代型ハイパラメーターフローサイトメーター等の最先端の解析技術を駆使して、個体から単一細胞レベルまでの高解像度解析を行い、加齢に伴う免疫老化現象の量的・質的変化を総合的に評価する系の構築を目指しています(参考資料はこちら)。さらに加齢に伴う免疫機能低下の改善法を見出し、特に高齢者向け感染症ワクチン、がん免疫療法の開発に繋げていきます。
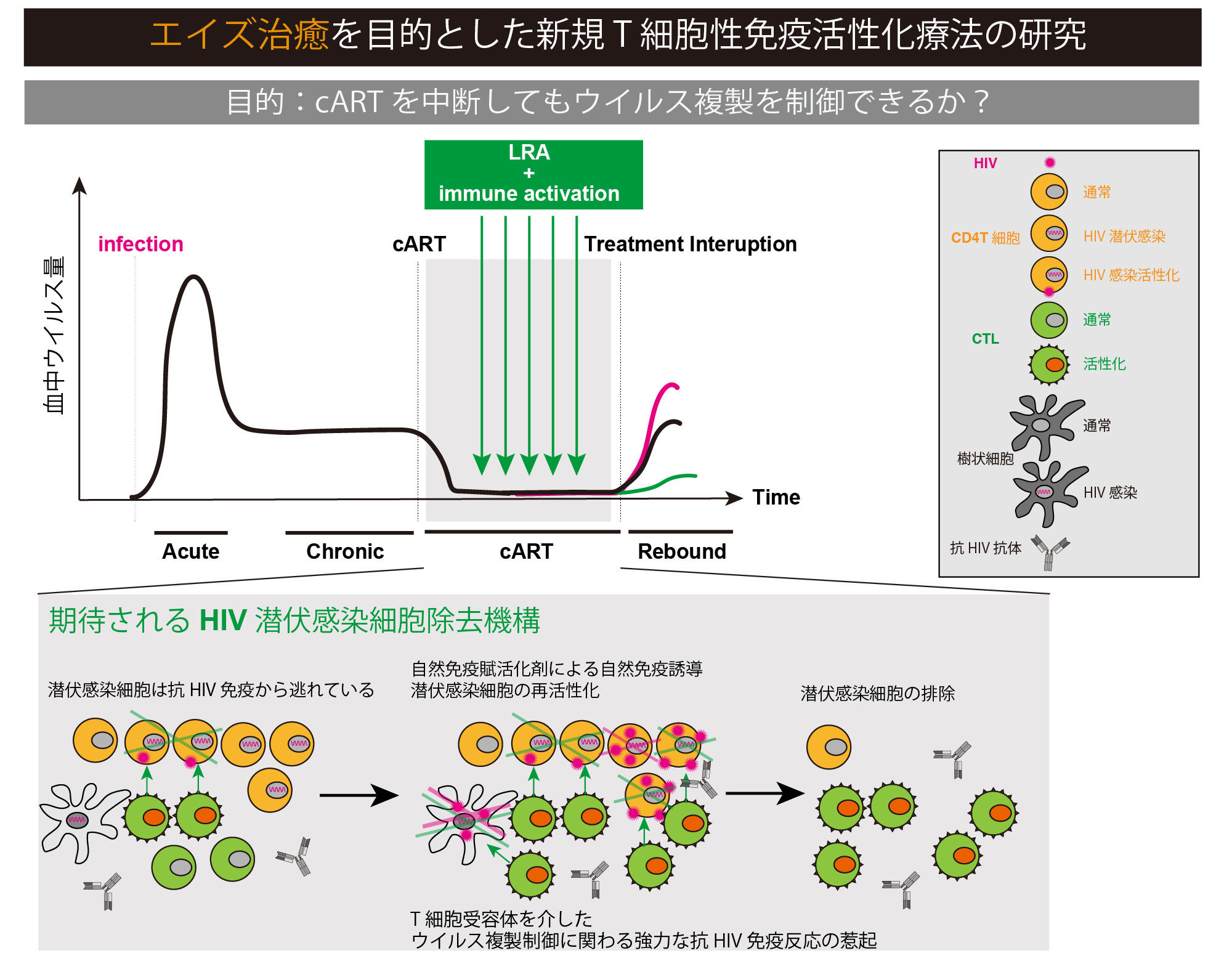
HIVは後天性免疫不全症候群(エイズ)の原因ウイルスであり、同定されてから30年以上経過した現在でも、全世界で約3500万人感染者がいます。日本国内においては感染者数が増加傾向にあり、2万人近い感染者がいると考えられ、依然として重大な新興・再興感染症の一つです。エイズ治療に関しては、これまで複数の抗レトロウイルス薬が開発され、また多剤併用療法(cART)が確立されたことで、血中ウイルス量を検出限界以下にコントロールできるようになりましたが、一方で体内からウイルス潜伏感染細胞を完全に除去する事はできず、cARTを開始すると一生涯薬を飲み続けなければなりません。つまりHIV-1治療において、cART治療後も体内に残る潜伏感染細胞を排除することが、いわゆる機能的治癒、エイズ根治に繋がると考えられます。 この機能的治癒を達成するためには、1) 潜伏感染細胞を再活性化させ、細胞変性効果(CPE)による感染細胞死を誘導すること、2) CD8 T細胞を中心とする抗HIV-1免疫反応の強力な活性化を誘導することが重要性です。そこで我々は現行cARTと合わせて行う、上記2つの免疫反応を強力に誘導することのできる新規免疫賦活化療法の確立を目指し研究を行なっています。
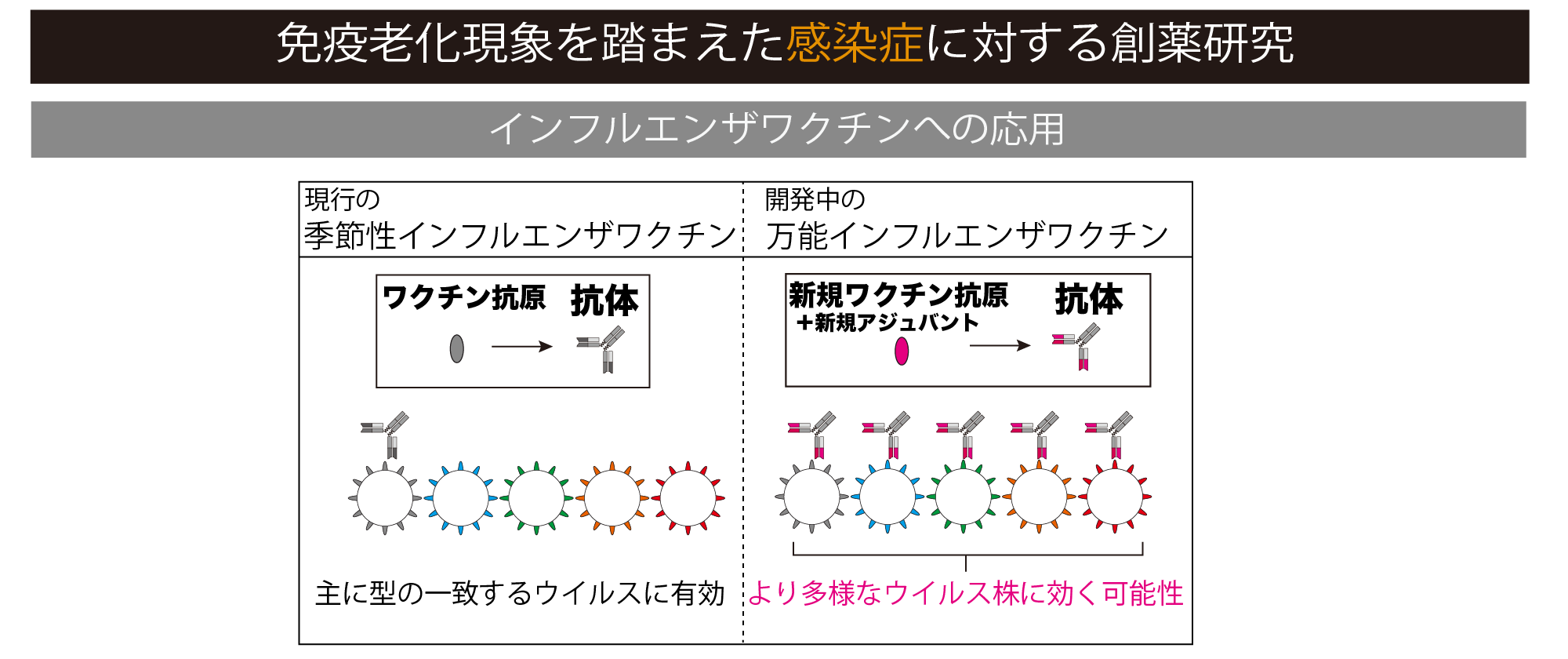
インフルエンザは、インフルエンザウイルスを病原体とする感染症です。毎年世界各地で流行がみられ、毎年約1500万人前後がインフルエンザに罹患しています。インフルエンザウイルスには多型があり、特にA型とB型が世界的な流行を示しています。ウイルス粒子の表面には糖タンパク質であるヘマグルチニン(HA)とノイラミニダーゼ(NA)が突出しており、その組み合わせにより複数の亜型(H1N1、H3N2、H5N1など)が存在し、非常に多様性に富んだウイルスであることが知られています。現行の季節性インフルエンザワクチンとして用いられているスプリット型ワクチンは、流行する型を予測し、一般的にはH1N1から1種類、H3N2から1種類、B型から2種類、合計4種類のウイルス糖タンパク質に標的を定めた4価ワクチンとなっています。しかしながら、HAは変異が生じやすく、変異が生じたウイルスにはワクチン効果は有効ではないため、変異ウイルス株にも対応可能なワクチン開発は急務となっています。加えて、高齢化社会が進行するにつれ、高齢者における感染症対策の一環としての効果的なインフルエンザワクチンの開発ニーズは高まっています。 我々は国立感染症研究所と大日本住友製薬株式会社との共同研究において、従来の製造方法とは異なったワクチン抗原と、大日本住友製薬株式会社において独自に開発中のアジュバントを組み合わせた万能インフルエンザワクチンの開発研究を行なっています。この万能インフルエンザワクチンのウイルス抗原の精製方法は、国立感染症研究所免疫部の高橋先生のグループにより開発されたもので、ワクチンにより「HA抗原の中でも変異が起きにくく、かつ異なるHA 型のウイルス間でも保存された領域に対する抗体」を誘導できる可能性が示唆されています。このワクチン抗原に大日本住友製薬株式会社により開発中の新規アジュバントを組み合わせることで、夢の万能インフルエンザワクチン開発の実現を目指しています。我々のグループは、本ワクチンの実用化に向け、特に霊長類モデルにおける免疫学的解析を次世代型ハイパラメーターフローサイトメーターを駆使して行い、その安全性と有効性を評価することで、本共同研究に貢献しています。
準備中

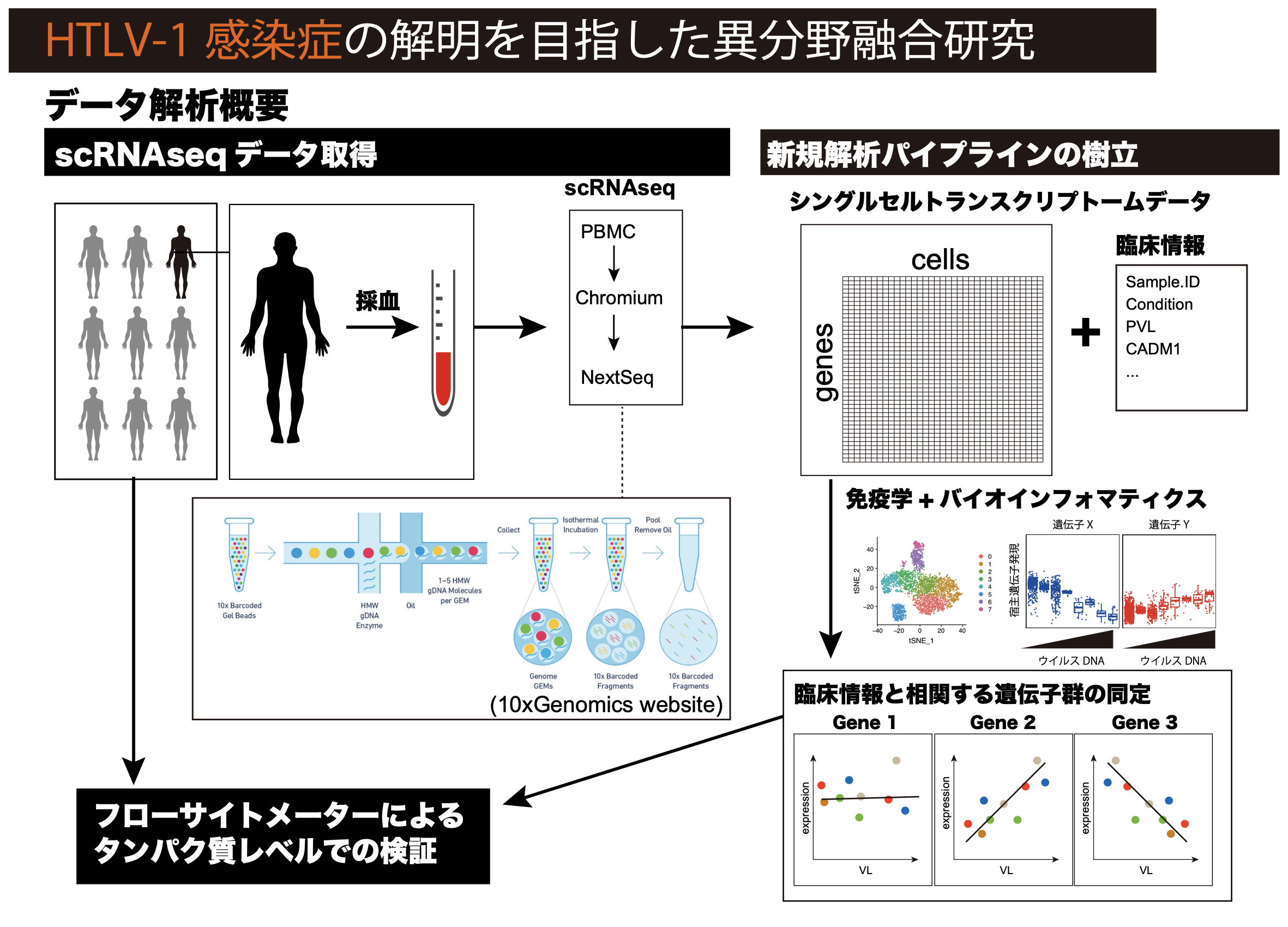
HTLV-1(human T-cell Leukemia Virus Type I:ヒトT細胞白血病ウイルス)は、血液中の白血球のうち、リンパ球に慢性持続感染するウイルスです。感染経路は、母乳や性交渉を介したものであり、一般的な日常生活で感染が広がるものではありません。また、HTLV-1に感染した方のうちのほとんど(~95%)は生涯病気になりませんが、一部の感染者は、ATL (Adult T-cell Leukemia:成人T細胞白血病)という難治性の血液のがんやHAM(HTLV-1 Associated Myelopathy: HTLV-1関連脊髄症)、TSP(Tropical Spastic Paraparesis: 熱帯性痙性麻痺)といった難治性の慢性炎症性疾患を発症します。このウイルスは、世界の中でも日本、特に九州・沖縄地方での感染者が多く、世界に先駆けて日本が取り組むべく課題であると我々は考えています。 これまでに、基礎・臨床両面において数多くの研究が行われてきましたが、依然として、ATL/HAM/TSPの発症機構は不明であり、我々は、異分野融合の新しいアプローチによりその本態に迫ろうと試みています。具体的には、熊本大学ヒトレトロウイルス学共同研究センターの佐藤賢文教授とともに、ATL/HAM/TSP発症に関与する因子(群)を明らかにする目的で、HTLVキャリア由来のPBMCを用いたシングルセルトランスクリプトーム解析による遺伝学的方法論とマルチカラーフローサイトメーター解析を通じた免疫学的方法論とを融合した新しい方法により、HTLV-1関連疾患の病態予測サロゲートマーカーの探索を進めています。
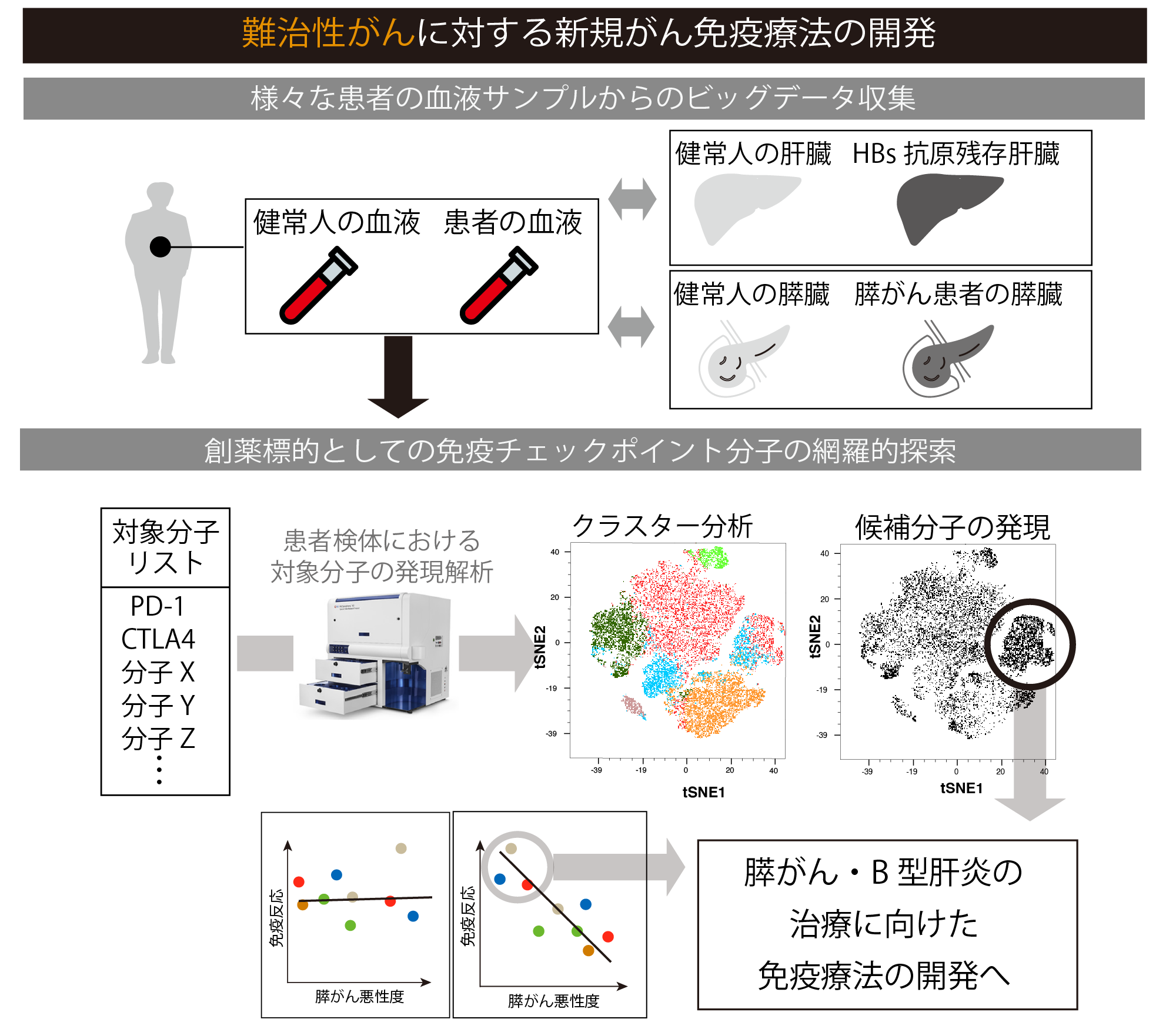
膵臓がんは消化器がんの中でも非常に予後が悪く、全体の5年生存率は10%に満たないとも言われていますが、その最大の理由は、早期診断が極めて難しいという点です。これまでにも早期診断マーカーを発見するために、たくさんの研究が行われてきましたが、既存のものより有用な腫瘍マーカーはいまだ見つかっておらず、診断時に唯一の根治治療である手術療法の適応になるのはわずか30-40%というのが現状です。さらに、抗がん剤が効きにくく、有効な抗がん剤の種類も少ない点も膵臓がんが予後不良である原因の一つです。また、近年、他癌では有用性が認められている多くの分子標的治療剤や、免疫療法も、膵臓がんにおいてはその有効性が乏しいことが分かっています。 なぜ膵臓がんはこのような治療抵抗性を示すのか?膵臓がんに罹った状態で生体にどのような免疫反応が起こっているのかを含め、その病態を解明することは、今後、膵臓がんに対する有効な治療法を確立していくためにも非常に重要であると考えられます。 我々は大阪大学外科学講座消化器外科学教室との共同研究により、膵臓がんの患者さんの様々な時相における血液中の血球(主にTリンパ球)のプロファイルを次世代型ハイパラメーターフローサイトメーターを用いて解析し、膵臓がんに対する免疫応答反応のメカニズム解明を目指しています。さらにそれら研究成果から、膵臓がんに対する早期診断、治療効果判定、予後予測などに有用となるマーカーの同定を試みます。
HBVはB型肝炎の原因ウイルスであり、HBV感染によるB型慢性肝炎患者の自然経過においては、約90%は進展せず、約10%でのみ肝硬変、肝がんへと進展していきます。これら病態を決定する要因の一つとして、免疫反応の関与が示唆されています。 加えて成人期に初感染すると、免疫系が正常の場合は95%の症例でHBVは排除されることや、HBVワクチンに一定の効果があることから、HBV制御における免疫反応の重要性を疑う余地はありません。他方、現在のB型慢性肝炎・肝硬変の治療には主に核酸アナログが用いられ、HBVDNA量の低下によって肝硬変や肝がんへの進行はある程度の抑制が可能となっています。しかしながら、核酸アナログを長期間服用しても、約3-4%しかHBs抗原が消失しないのが現状です。つまり核酸アナログにより血中のHBV DNAが検出感度以下になっても、多くの症例ではHBV複製鋳型やHBVゲノムは肝細胞に残存しており、これが原因となって肝がんをきたすことがあります。 それゆえ現在の臨床的な治療目標は、発癌リスクと相関すると考えられるHBs抗原の消失です。我々はfunctional cure(機能的治癒)を達成するために、まず核酸アナログによる治療によりHBV DNAを検出限界以下へと減らし、その上で残されたHBV感染細胞を免疫反応により排除することを目指して、国立国際医療センター肝炎免疫研究センターをはじめとする多くの国内共同研究先と密接に連携し、本研究を展開しています。